IНСТРУКЦІЯ
для медичного застосування лікарського засобу
ПЕНТАСА
(PENTASA®)
Склад:
діюча речовина:месалазин;
100 мл суспензії містять месалазину1 г;
допоміжні речовини: динатрію едетат (Трилон Б); натрію метабісульфіт (Е 223); натрію ацетат, тригідрат; кислота хлористоводнева концентрована; вода очищена.
Лікарська форма.Суспензія ректальна.
Основні фізико-хімічні властивості:суспензія від білого до жовтуватого кольору.
Фармакотерапевтична група.Протизапальні засоби, що застосовуються при захворюваннях кишечнику. Кислота аміносаліцилова та подібні засоби. Месалазин.
Код АТХ А07Е С02.
Фармакологічні властивості.
Фармакодинаміка.
Месалазин – активний компонент сульфасалазину, який застосовують для лікування виразкового коліту і хвороби Крона.
Клінічні дослідження свідчать, що терапевтичні властивості месалазину при пероральному та ректальному застосуванні обумовлені більшою мірою його місцевою дією на запалені ділянки кишечнику, аніж системним ефектом.
Існує інформація про те, що тяжкість запалення кишечнику у хворих із виразковим колітом, які отримували месалазин, є обернено корельована концентрацією месалазину в слизовій оболонці.
У пацієнтів із запальними захворюваннями кишечнику спостерігаються підвищення міграції лейкоцитів, аномальне продукування цитокінів, збільшення продукування метаболітів арахідонової кислоти (особливо лейкотрієнів В4), збільшення концентрації вільних радикалів у запалених тканинах кишечнику.
Механізм дії месалазину не є повністю зрозумілим, але залучено такі механізми, як активація γ-форми рецепторів, активованих проліфераторами пероксисом (PPAR-γ), та інгібування ядерного фактора-каппа B (NF-κB) в слизовій оболонці кишечнику.
Фармакологічний ефект месалазину у ході дослідженьin vitro таin vivo полягає у пригніченні хемотаксису лейкоцитів, зменшенні продукування цитокінів і лейкотрієнів та нейтралізації вільних радикалів. На сьогодні невідомо, які з цих механізмів відіграють провідну роль у клінічній ефективності месалазину.
Фармакокінетика.
Терапевтична дія месалазину в основному визначається його місцевим контактом з ділянкою запалення слизової оболонки кишечнику.
Застосування ректальної суспензії забезпечує високу концентрацію месалазину в дистальному відділі шлунково-кишкового тракту та низьку системну абсорбцію. Встановлено, що ректальна суспензія досягає низхідної ободової кишки та розповсюджується по її слизовій.
Абсорбція. Абсорбція після ректального застосування є низькою, залежить від дозування та ступеня дисперсності. Вимірювання кількості месалазину в сечі здорових добровольців за умови застосування 2 г на добу (двічі по 1 г) препарату Пентаса показало, що приблизно 15–20 % дози поглинається.
Розподіл. Зв’язування месалазину з білками плазми становить приблизно 50 %, а ацетил-месалазину – приблизно 80 %.
Біотрансформація. Месалазин перетворюється на N-ацетил-месалазин (ацетил-месалазин) як пресистемно у слизовій оболонці кишечнику, так системно в печінці, переважно за допомогою NAT-1. Незначне ацетилювання здійснюється за участю бактерій товстого кишечнику. Ацетилювання месалазину, ймовірно, не пов’язане з фенотипом ацетилювання пацієнта.
Також вважається, що ацетил-месалазин є клінічно та токсикологічно неактивним, хоча ці дані точно не підтверджені.
Виведення.Через безперервне вивільнення месалазину з препарату Пентаса в шлунково-кишковому тракті після перорального прийому період напіввиведення неможливо визначити. Проте після того, як сполука зникає з ШКТ, період напіввиведення месалазину з плазми крові після перорального або внутрішньовенного прийому становить 40 хвилин, а для ацетил-месалазину – приблизно 70 хвилин.
Особливі групи пацієнтів
Патофізіологічні зміни, такі як діарея та підвищена кислотність кишечнику, що спостерігаються під час активного запального захворювання кишечнику, мають лише незначний вплив на транспортування месалазину до слизової оболонки кишечнику після перорального застосування. Екскреція з сечею 20–25 % добової дози спостерігається в осіб з прискореним кишковим транзитом. Аналогічно – спостерігається відповідне збільшення екскреції з фекаліями.
Системний вплив після введення ректальної суспензії Пентаса значно нижчий у пацієнтів з активним виразковим колітом порівняно з пацієнтами в стадії ремісії.
Клінічні характеристики.
Показання.
Виразковий проктосигмоїдит та лівобічний коліт.
Протипоказання.
Підвищена чутливість до месалазину, саліцилатів або до будь-якої з допоміжних речовин. Тяжка печінкова або ниркова недостатність.
Взаємодія з іншими лікарськими засобами та інші види взаємодій.
Одночасне застосування з іншими відомими нефротоксичними засобами, такими як НПЗЗ або азатіоприн, може збільшити ризик небажаних реакцій з боку нирок.
Під час комплексного лікування препаратом Пентаса і азатіоприном, 6-меркаптопурином або тіогуаніном у деяких дослідженнях було виявлено більшу частоту мієлосупресивних ефектів, що, ймовірно, свідчить про наявність взаємодії, однак механізм взаємодії встановлений не повністю. Рекомендований регулярний контроль за рівнем лейкоцитів і дотримання відповідного режиму дозування для тіопуринів.
Докази того, що месалазин може знизити антикоагуляційну дію варфарину, слабкі.
Особливості застосування.
Пацієнти, які мають в анамнезі реакції гіперчутливості на лікарські засоби, що містять сульфасалазин, повинні знаходитися під ретельним наглядом лікаря на початку застосування лікарського засобу Пентаса (ризик алергії до саліцилатів).
Ідіопатична внутрішньочерепна гіпертензія
Повідомлялося про ідіопатичну внутрішньочерепну гіпертензію (псевдопухлина головного мозку) у пацієнтів, які застосовували месалазин. Пацієнтів слід попередити про ознаки та симптоми ідіопатичної внутрішньочерепної гіпертензії, включаючи сильний або рецидивуючий головний біль, порушення зору або шум у вухах. У разі виникнення ідіопатичної внутрішньочерепної гіпертензії слід розглянути питання про припинення застосування месалазину.
Тяжкі побічні реакції з боку шкіри
Повідомлялося про тяжкі шкірні побічні реакції (ТШПР), включаючи індуковану лікарськими засобами еозинофілію з системними симптомами (DRESS-синдром),синдром Стівенса-Джонсона (ССД) і токсичний епідермальний некроліз (ТЕН), пов’язаних із лікуванням месалазином.
У разі появи перших ознак та симптомів тяжких побічних реакцій з боку шкіри, таких як шкірний висип, ураження слизової оболонки або інших ознак гіперчутливості, включаючи гострі реакції непереносимості, а саме: коліки у животі, гострий біль у животі, підвищення температури тіла, сильний головний біль – лікування слід негайно припинити.
З обережністю слід застосовувати хворим із порушенням функції печінки. На розсуд лікаря до та протягом лікування слід контролювати функціональні показники печінки, такі як АлАТ та АсАТ.
Препарат не рекомендується застосовувати пацієнтам з нирковою недостатністю. Слід регулярно контролювати функцію нирок (рівень креатиніну у сечі та сироватці, осад сечі), особливо на початку лікування. Необхідно визначити урологічний статус пацієнта (тест-смужки) до та під час лікування на розсуд лікаря. Аналізи рекомендується робити через 2 тижні після початку лікування і надалі 2–3 рази з інтервалом 4 тижні. Якщо результати досліджень у межах норми, періодичні дослідження можна проводити кожні три місяці. У разі появи додаткових симптомів ці дослідження слід виконати негайно.
У пацієнтів, у яких протягом лікування розвивається порушення функції нирок, слід запідозрити месалазиніндуковану нефротоксичність. Одночасне застосування інших відомих засобів з підтвердженим нефротоксичним ефектом потребує частішого контролю за функцією нирок.
Повідомлялося про випадки нефролітіазу при застосуванні меалазину, включаючи камені із 100 % вмістом месалазину. Рекомендовано забезпечити достатній водний режим під час лікування.
Пацієнти з легеневими захворюваннями, зокрема астмою, повинні перебувати під ретельним контролем протягом курсу лікування (див. розділ «Побічні реакції»).
Про месалазиніндуковані серцеві реакції гіперчутливості (міо- та перикардит) повідомлялося рідко.
Дуже рідко повідомлялося про серйозну дискразію крові, пов’язану із застосуванням месалазину. Перед початком і під час лікування на розсуд лікаря рекомендовано провести аналіз крові для підрахунку окремих видів лейкоцитів. Одночасне лікування з месалазином може збільшити ризик дискразії крові у пацієнтів, що отримують азатіоприн або 6-меркаптопурин, або тіогуаніну (див. розділ «Взаємодія з іншими лікарськими засобами та інші види взаємодій»). Лікування слід припинити при підозрі або підтвердженні цих побічних реакцій.
Будь-який невикористаний лікарський засіб та відходи слід утилізувати згідно з місцевими вимогами.
Месалазин може викликати червоно-коричневе забарвлення сечі після контакту з відбілювачем на основі гіпохлориту натрію (наприклад, у туалетах, очищених гіпохлоритом натрію, що міститься в деяких відбілювачах).
Ректальна суспензія Пентаса може забарвлювати білизну та постіль.
Застосування в період вагітності або годування груддю.
Лікарський засіб Пентаса під час вагітності та годування груддю потрібно застосовувати з обережністю і тільки тоді, коли, на думку лікаря, очікувана користь для вагітної перевищує потенційний ризик для плода. Сам основний стан – запальне захворювання кишечнику (ЗЗК) – може вплинути на результат вагітності.
Належні дані щодо застосування лікарського засобу вагітним жінкам відсутні. Однак результати обмеженої кількості експозицій препарату під час вагітності свідчать про відсутність побічного впливу месалазину на перебіг вагітності або на здоров’я плода/новонародженого. На сьогодні відсутні інші відповідні епідеміологічні дані.
Вагітність.
Відомо, що месалазин проникає крізь плацентарний бар’єр і його концентрації в плазмі пуповини нижчі, ніж концентрації в плазмі матері. Метаболіт ацетил-месалазин виявлений в однакових концентраціях в пуповині і плазмі матері. Дослідження перорального застосування месалазину на тваринах не вказує на прямий чи непрямий шкідливий вплив на вагітність, розвиток ембріона та плода, пологи та постнатальний розвиток. Не існує адекватних та добре контрольованих досліджень застосування лікарського засобу Пентаса вагітним. Обмежені дані застосування месалазину не свідчать про збільшення загальної частоти вроджених вад розвитку у людей. Деякі дані свідчать про збільшення частоти передчасних пологів, мертвонародження та низької маси тіла при народженні, однак ці небажані результати вагітності також пов’язані з активною стадією запальних захворювань кишечнику.
Були повідомлення про порушення з боку системи крові (панцитопенія, лейкопенія, тромбоцитопенія, анемія) у новонароджених, матері яких застосовували лікарський засіб Пентаса.
В одному випадку після тривалого застосування високих доз месалазину (2–4 г перорально) під час вагітності повідомлялося про ниркову недостатність у новонародженого.
Період годування груддю.
Месалазин проникає в грудне молоко. Концентрація месалазину в грудному молоці нижча, ніж в крові матері, тоді як метаболіт – ацетил-месалазин – виявляється в аналогічних або вищих концентраціях. Існує обмежений досвід перорального застосування месалазину жінкам, які годують груддю. Не проводилося контрольованих досліджень застосування препарату Пентаса під час годування груддю. Не можна виключити реакцій гіперчутливості, таких як діарея, у новонародженого. Якщо у дитини з’являється діарея, грудне вигодовування слід припинити.
Фертильність
Дані щодо застосування месалазину тваринам не показують впливу на чоловічу або жіночу фертильність.
Здатність впливати на швидкість реакції при керуванні автотранспортом або іншими механізмами.
Лікування препаратом Пентаса не впливає на здатність керувати транспортними засобами і/або працювати з іншими механізмами.
Спосіб застосування та дози.
1 клізма перед сном.
Перед застосуванням клізми рекомендується випорожнити кишечник.
Клізма поміщена в пакет з алюмінієвої фольги.
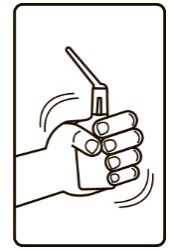 1. Безпосередньо перед застосуванням дістати флакон із пакета з алюмінієвої фольги та добре струснути.
1. Безпосередньо перед застосуванням дістати флакон із пакета з алюмінієвої фольги та добре струснути.
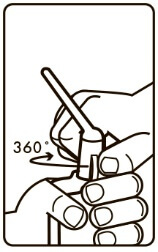 2. Щоб зламати засіб закупорювання, слід повернути наконечник на один повний оберт (після повороту наконечник повинен бути в тому ж положенні, що й перед поворотом).
2. Щоб зламати засіб закупорювання, слід повернути наконечник на один повний оберт (після повороту наконечник повинен бути в тому ж положенні, що й перед поворотом).

3. Помістити руку в один із поліетиленових пакетів, що містяться в упаковці.
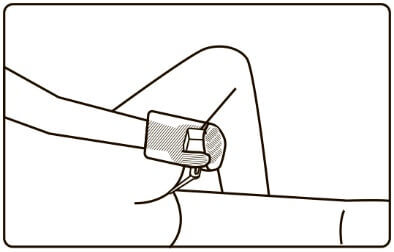
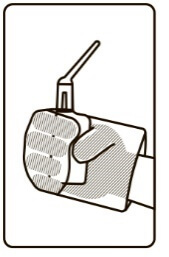 4. Тримати контейнер, як показано на рисунку на пакеті.
4. Тримати контейнер, як показано на рисунку на пакеті.
 5. Для введення клізми лягти на лівий бік, ліва нога пряма, а права – зігнута вперед для рівноваги. Обережно ввести кінчик аплікатора у пряму кишку. Підтримувати достатнє постійне натискання рукою у міру розподілу вмісту клізми. Вміст флакона слід використати максимально протягом 30–40 секунд.
5. Для введення клізми лягти на лівий бік, ліва нога пряма, а права – зігнута вперед для рівноваги. Обережно ввести кінчик аплікатора у пряму кишку. Підтримувати достатнє постійне натискання рукою у міру розподілу вмісту клізми. Вміст флакона слід використати максимально протягом 30–40 секунд.
6. Як тільки флакон спорожніє, вийняти наконечник з флаконом, все ще стискаючи його.
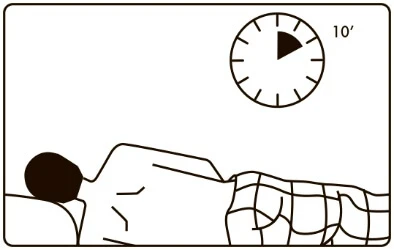 7. Суспензія повинна залишатися в кишечнику. Пацієнту слід залишатися в розслабленому стані в вищезазначеному положенні ще 5–10 хвилин або допоки пройде позив.
7. Суспензія повинна залишатися в кишечнику. Пацієнту слід залишатися в розслабленому стані в вищезазначеному положенні ще 5–10 хвилин або допоки пройде позив.
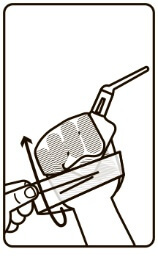 8. Згорнути поліетиленовий пакет поверх порожнього флакона. Викинути його і вимити руки.
8. Згорнути поліетиленовий пакет поверх порожнього флакона. Викинути його і вимити руки.
Пацієнти літнього віку
Зниження дози пацієнтам літнього віку не потрібне, але рекомендується обережність при застосуванні та контроль функції нирок.
Інформацію про застосування пацієнтам з порушенням функції нирок та/або печінки див. у розділах «Протипоказання» та «Особливості застосування».
Діти.Є обмежені клінічні дані щодо ефективності лікування дітей.
Передозування.
Одноразова внутрішньовенна доза месалазину 920 мг/кг у щурів та одноразова пероральна доза до 5 г/кг у свиней не були летальними.
Існує обмежений клінічний досвід передозування препаратом Пентаса, який не вказує на ниркову або печінкову токсичність.
Оскільки Пентаса є аміносаліцилатом, то можуть з’явитися симптоми токсичності саліцилатів, такі як порушення кислотно-лужної рівноваги, гіпервентиляція, набряк легень, блювання, дегідратація та гіпоглікемія. Симптоми, викликані передозуванням саліцилатами, добре описані в медичній літературі.
Були повідомлення про пацієнтів, які щоденно приймали 8 г месалазину протягом місяця без будь-яких побічних явищ.
Лікування передозування у людини
Оскільки немає специфічного антидоту, лікування передозування підтримувальне та симптоматичне. Лікування у стаціонарі включає ретельний контроль за функцією нирок.
Побічні реакції.
Побічні реакції, що найчастіше спостерігалися у ході клінічних досліджень: діарея, нудота, біль у животі, головний біль, блювання і висипання. Іноді спостерігаються реакції гіперчутливості та медикаментозна гарячка.
У зв’язку з лікуванням месалазином повідомлялося про тяжкі шкірні побічні реакції (ТШПР), включаючи індуковану лікарськими засобами еозинофілію з системними симптомами (DRESS-синдром), синдром Стівенса-Джонсона (ССД) і токсичний епідермальний некроліз (ТЕН) (див. розділ «Особливості застосування»).
Після ректального введення можливі місцеві реакції, такі як свербіж, ректальний дискомфорт та позиви до дефекації.
Частота побічних ефектів базується на клінічних дослідженнях та звітах у післяреєстраційний період і визначена таким чином: часто (≥ 1/100, < 1/10), нечасто (≥ 1/1000, < 1/100), рідко (≥ 1/10000, < 1/1000), дуже рідко (< 1/10000), частота невідома (неможливо встановити на основі наявних даних).
З боку крові та лімфатичної системи:дуже рідко – зміна показників крові (анемія, апластична анемія, агранулоцитоз, нейтропенія, лейкопенія (у т.ч. гранулоцитопенія), панцитопенія, тромбоцитопенія та еозинофілія, як складова алергічної реакції).
З боку імунної системи: дуже рідко – реакції гіперчутливості, включаючи алергічну екзантему і DRESS-синдром, медикаментозна гарячка.
З боку нервової системи:часто – головний біль; рідко – запаморочення; дуже рідко – периферична нейропатія; частота невідома - ідіопатична внутрішньочерепна гіпертензія (див. розділ «Особливості застосування»).
З боку серця:рідко – міо*- та перикардит*.
З боку дихальної системи, органів грудної клітки та середостіння:діже рідко – алергічні та фібротичні легеневі реакції (у т.ч. задуха, кашель, бронхоспазм, алергічний альвеоліт, легенева еозинофілія, інтерстиціальна легенева хвороба, легеневі інфільтрати, пневмоніт).
З боку шлунково-кишкового тракту:часто – діарея, біль у животі, нудота, блювання; рідко – підвищений рівень амілази, гострий панкреатит*, метеоризм; дуже рідко – панколіт.
З боку печінки і жовчовивідних шляхів:дуже рідко – підвищений рівень ферментів печінки, параметрів холестазу (а саме: лужної фосфатази, гамма-глутамілтрансферази і білірубіну), гепатотоксичність (у т. ч. гепатит*, холестатичний гепатит, цироз, печінкова недостатність).
З боку шкіри та підшкірних тканин:часто – висипання(у т. ч. кропив’янка та еритематозне висипання); рідко – світлочутливість**; дуже рідко – алопеція оборотна, алергічний дерматит, мультиформна еритема; частота невідома – синдром Стівенса – Джонсона (SJS), токсичний епідермальний некроліз (ТЕN); індукована лікарськими засобами еозинофілія з системними симптомами (DRESS-синдром).
З боку кістково-м’язової системи та сполучної тканини:дуже рідко - міалгія, артралгія, реакції, подібні до еритематозного вовчака.
З боку нирок і сечовидільної системи:дуже рідко – порушення функції нирок (у т. ч. гострий і хронічний інтерстиціальний нефрит*, нефротичний синдром, ниркова недостатність); частота невідома – нефролітіаз***, зміна кольору сечі***.
З боку репродуктивної системи:дуже рідко – олігоспермія (оборотна).
Загальні порушення і порушення у місці введення:часто – свербіж; нечасто – анальний дискомфорт і подразнення у місці введення, тенезми; дуже рідко – лихоманка.
*Механізм розвитку месалазиніндукованого міо- і перикардиту, панкреатиту, нефриту і гепатиту невідомий, але можливе його алергічне походження. Слід взяти до уваги, що деякі із цих захворювань можуть бути пов’язані із запальним захворюванням кишечнику.
** Світлочутливість: більш серйозні реакції спостерігаються у пацієнтів із наявними захворюваннями шкіри, такими як атопічний дерматит та атопічна екзема.
***Див. розділ «Особливості застосування» для отримання додаткової інформації.
Повідомлення про підозрювані побічні реакції
Повідомлення про побічні реакції після реєстрації лікарського засобу має важливе значення. Це дає змогу проводити моніторинг співвідношення користь/ризик при застосуванні цього лікарського засобу. Медичним та фармацевтичним працівникам, а також пацієнтам або їхнім законним представникам слід повідомляти про усі випадки підозрюваних побічних реакцій та відсутності ефективності лікарського засобу через Автоматизовану інформаційну систему з фармаконагляду за посиланням: https://aisf.dec.gov.ua.
Термін придатності.3 роки.
Умови зберігання.Зберігати при температурі 15–25 °С в оригінальній упаковці. Зберігати у недоступному для дітей місці.
Упаковка.По 100 мл суспензії у флаконі з наконечником і внутрішнім клапаном; по 1 флакону у пакеті з алюмінієвої фольги; по 5 або 7 флаконів та 5 або 7 поліетиленових пакетів у картонній упаковці.
Категорія відпуску.За рецептом.
Виробник.Феррінг-Лечива, а.с., Чеська Республіка / Ferring-Leciva, a.s., Czech Republic.
Місцезнаходження виробника та адреса місця провадження його діяльності.
К Рибніку 475, Джесеніце в Празі, 252 42, Чеська Республіка / K Rybniku 475, Jesenice u
Prahy, 252 42, Czech Republic.